Die Erwartungshaltung des aufgeklärten Tierbesitzers und somit auch der Erfolgsdruck auf den Praktiker steigen, da die Methoden zur Krebsbehandlung immer effizienter werden.
Der Zeitpunkt jedoch, an dem die Behandlungseffizienz einer bösartigen Tumorerkrankung gemindert oder sogar nachteilig beeinflusst wird, ist meist, noch bevor die erste Tablette verabreicht, die erste Injektion gesetzt oder der erste Hautschnitt erfolgt ist.
Am Anfang steht die Diagnostik
Allgemein bekannt ist, dass vor der Therapie grundsätzlich immer erst die Diagnose stehen sollte. Im Fall der Onkologie setzt dies ein Wissen rund um die Biologie des Tumors voraus, sowie die diagnostischen Möglichkeiten und Fertigkeiten, die Ausbreitung der Erkrankung festzustellen.
Nur dadurch kann die Frage beantwortet werden, welcher Tumor wo überall im Körper nachzuweisen ist, welches die besten Therapieoptionen sind und mit welcher Prognose gerechnet werden kann. Mitunter führt eine umfangreiche Voruntersuchung auch zu der Entscheidung, dass nur noch palliative Maßnahmen gesetzt werden sollten oder es werden zusätzliche Erkrankungen gefunden, die eine Behandlung der ursprünglichen Diagnose verkomplizieren oder sogar unethisch bzw. unmöglich werden lassen.
Jedenfalls fordert der Umgang mit potenziellen Tumorpatienten und ihren Besitzern neben einem fundierten klinischen Wissen in besonderem Maße die soziale Kompetenz des Tierarztes und des beteiligten Personals (Moritz, 2013).
Es ist entscheidend, durch eine vollständige fachliche Aufklärung über die Erkrankung des Patienten dem Tierbesitzer eine Entscheidungsgrundlage zu liefern, anhand derer er die im Sinne des Tieres beste, aber mitunter weitreichende Entscheidung treffen kann. Erfolgt diese Aufklärung nicht bereits vor dem Beginn der Behandlung, ist man oftmals mit frustrierten Tierbesitzern konfrontiert, die ihre Erwartungshaltung nicht erfüllt sehen.
Was ist vom praktizierenden Onkologen vor Therapiestart alles zu beachten?
Anamnese und allgemeine Untersuchungen:
Bereits die Anamnese und das Signalement können entscheidende Hinweise auf eine bestimmte Tumorerkrankung liefern, beispielsweise aufgrund von Rasseprädispositionen, Alter, Geschlecht und Lebensumständen.
Eine umfangreiche klinische Gesamtbeurteilung des Patienten sollte stets einer speziellen onkologischen Abklärung vorausgehen, da die Körperkondition einen signifikanten Einfluss auf die Erfolgsaussichten der Tumortherapie und somit auf die Prognose hat. Ist die Allgemeinuntersuchung abgeschlossen, sollte aus onkologischer Sicht das erste Ziel sein, festzustellen, um welche Art Tumor es sich handelt.
Blutlaborwertuntersuchungen können mitunter einen zusätzlichen Hinweis in der Aufarbeitung neoplastischer Erkrankungen liefern, meistens sind die Abweichungen allerdings eher unspezifisch und führen nicht direkt zu einer Diagnose. Tumormarker haben sich nach wie vor nicht flächendeckend durchgesetzt und haben bei Hund und Katze derzeit wenig Bedeutung (Selvarajah et al., 2010).
Biopsie als Schlüssel zum Erfolg
Da viele Tumorlokalisationen der klinischen Untersuchung zugänglich sind, eignen sich diese bestens zur direkten Beprobung des Tumors.
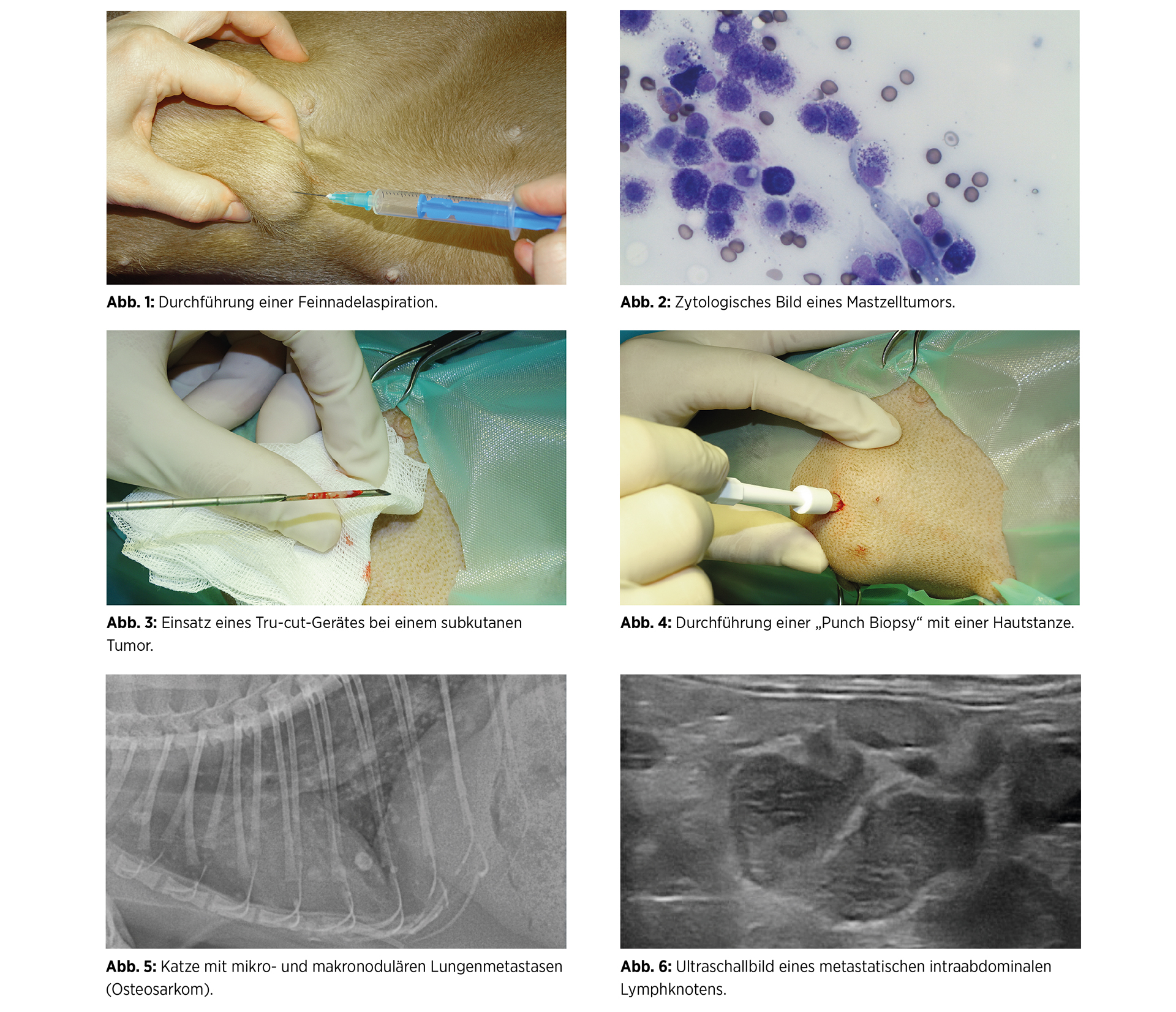
In vielen Fällen reicht die wenig invasive Methode der Feinnadelaspirationsbiopsie (FNAB) aus. Bei dieser Methode werden mittels dünner Einmalkanülen – weitestgehend schmerzfrei – Zellen aus dem veränderten Gewebe entnommen. Durchmesser der Kanüle und Ausmaß der Aspiration kann je nach Tumorlokalisation und zu erwartender Entität variieren. Nach Erfahrung des Autors ist in den meisten Fällen eine unarmierte Punktion mit einer 22G- oder 23G-Kanüle ausreichend, um genügend Zellen für eine Diagnosestellung zu gewinnen. Ob die gewonnenen Zellen im hauseigenen Labor mikroskopisch untersucht werden oder an ein Fremdlabor gesendet werden müssen, hängt von der Erfahrung des behandelnden Tierarztes ab. Lässt sich zytologisch keine klare Diagnose stellen, ist eine Biopsie des Tumors der nächste logische Schritt. Diese kann in der Regel in Sedierung und Lokalanästhesie durchgeführt werden, wobei unterschiedliche Techniken zur Anwendung kommen (Abb. 3+4).
Intrathorakale sowie intraabdominale Neoplasien können in der Regel gut unter Ultraschallkontrolle punktiert bzw. bioptiert werden, jedoch muss der Patientenbesitzer im Vorfeld über die Risiken aufgeklärt werden. Eine direkte chirurgische Entfernung eines Tumors ohne vorherige Diagnose darf nur dann erfolgen, wenn das biologische Verhalten (Dignität) keinen Einfluss auf das Ausmaß der Operation hat, was allerdings selten der Fall ist.
Bildgebende Verfahren im Tumorstaging
Nachdem die Tumorart festgestellt wurde, geht es nun darum, das lokale Ausmaß bzw. die Ausbreitung der Erkrankung festzustellen. Hierfür werden alle gängigen, verfügbaren diagnostischen Geräte wie Ultraschall, Röntgen, Computertomographie etc. herangezogen. Es gibt jedoch kein Routineprotokoll, nach dem vorgegangen werden kann. Abhängig von der Tumorbiologie macht es schließlich nur Sinn, Organe zu untersuchen, in die der Tumor in der Lage ist, abzuwandern. Ein profundes Fachwissen auf dem Gebiet der Kleintieronkologie hilft hier, dem Patienten „unnötige“ Untersuchungen zu ersparen, aber auch zeitgleich keine Tumorausbreitung zu übersehen, welche die Therapieentscheidung beeinflussen könnte.
Schnittbildverfahren (CT, MRI) sind in puncto Sensitivität meist Röntgenaufnahmen überlegen, vor allem im Bereich der Lungendiagnostik (Nemanic et al., 2006), allerdings auch mit höheren Kosten verbunden und nicht immer flächendeckend verfügbar. Wird eine Röntgenuntersuchung der Lunge zum Screening auf Metastasen durchgeführt, sollte diese in mindestens zwei Ebenen erfolgen, wobei eine beidseits latero-laterale (rechts und links anliegend) zu bevorzugen ist. Eine dritte Ebene kann zusätzliche Erkenntnisse bringen (Ober et al., 2006), der konkrete Nutzen der zusätzlichen Ebene wird jedoch kontrovers diskutiert. Zu beachten sind die unterschiedlichen röntgenologischen Erscheinungsformen von Lungenmetastasen, die vor allem bei der Katze oftmals zu Fehlinterpretationen führen können.
Bei der Ultraschalluntersuchung des Bauchraumes werden neben allen relevanten Organen auch die Lymphknoten in der Bauchhöhle evaluiert und bei entsprechender Veränderung ultraschallgestützt punktiert. Weiters kann die Sonographie auch zur Darstellung und assistierten Punktion von intrathorakalen oder subkutanen Neoplasien herangezogen werden. Der Einsatz von Ultraschallkontrastmitteln kann vor allem bei Veränderungen der Leber helfen, deren Dignität zu beurteilen (Kanemoto et al., 2009).
Nuklearmedizinische Verfahren (Szintigraphie, PET-CT), die in der Humanmedizin längst als Standard etabliert sind, konnten sich bis dato in der Veterinärmedizin nicht als routinemäßig eingesetztes Stagingtool durchsetzen und bleiben eher Einzelfällen vorbehalten.