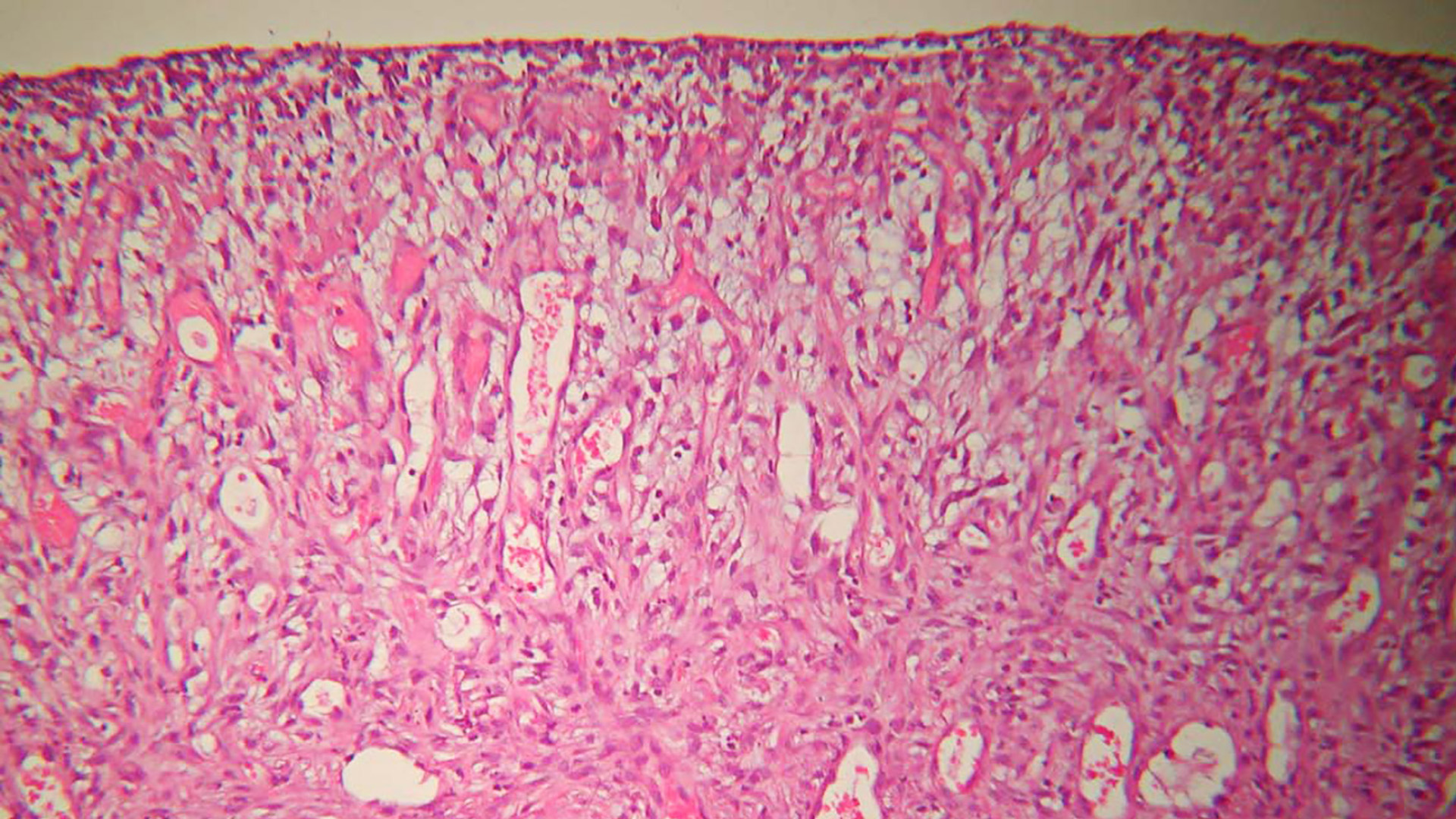
histologische Resektionsränder
Wem ist es nicht schon passiert, dass ein bereits resezierter Tumor wieder nachgewachsen ist, obwohl laut histologischem Befund die „Resektion im Gesunden“ erfolgt ist? Ein solches Erlebnis lässt sowohl den Tierarzt als auch den Tierbesitzer etwas ratlos zurück, wenn die methodischen Grenzen einer Untersuchung nicht bekannt sind. Diese sollen im Folgenden anhand des histologischen Pro-zederes näher erläutert werden.
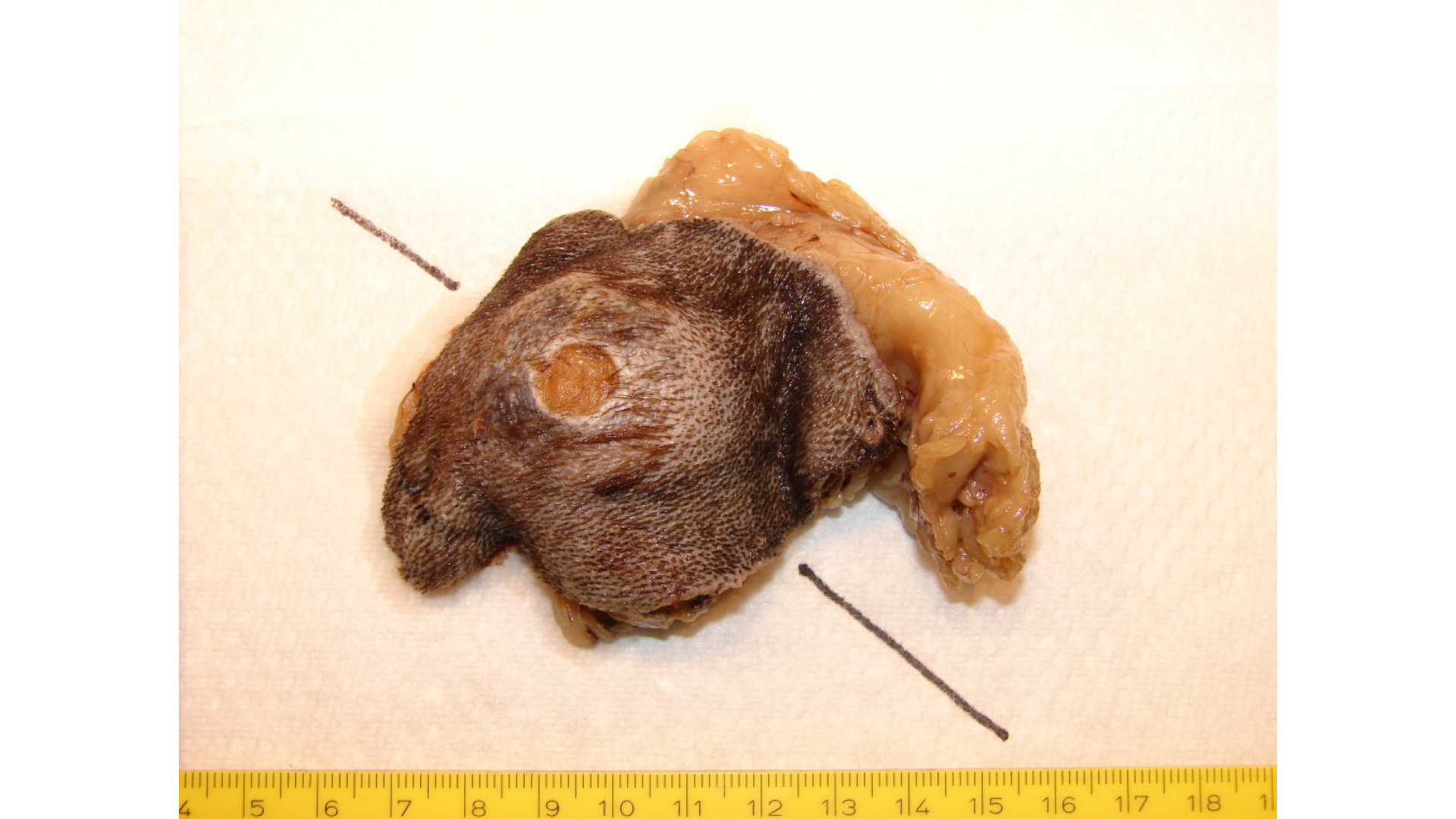
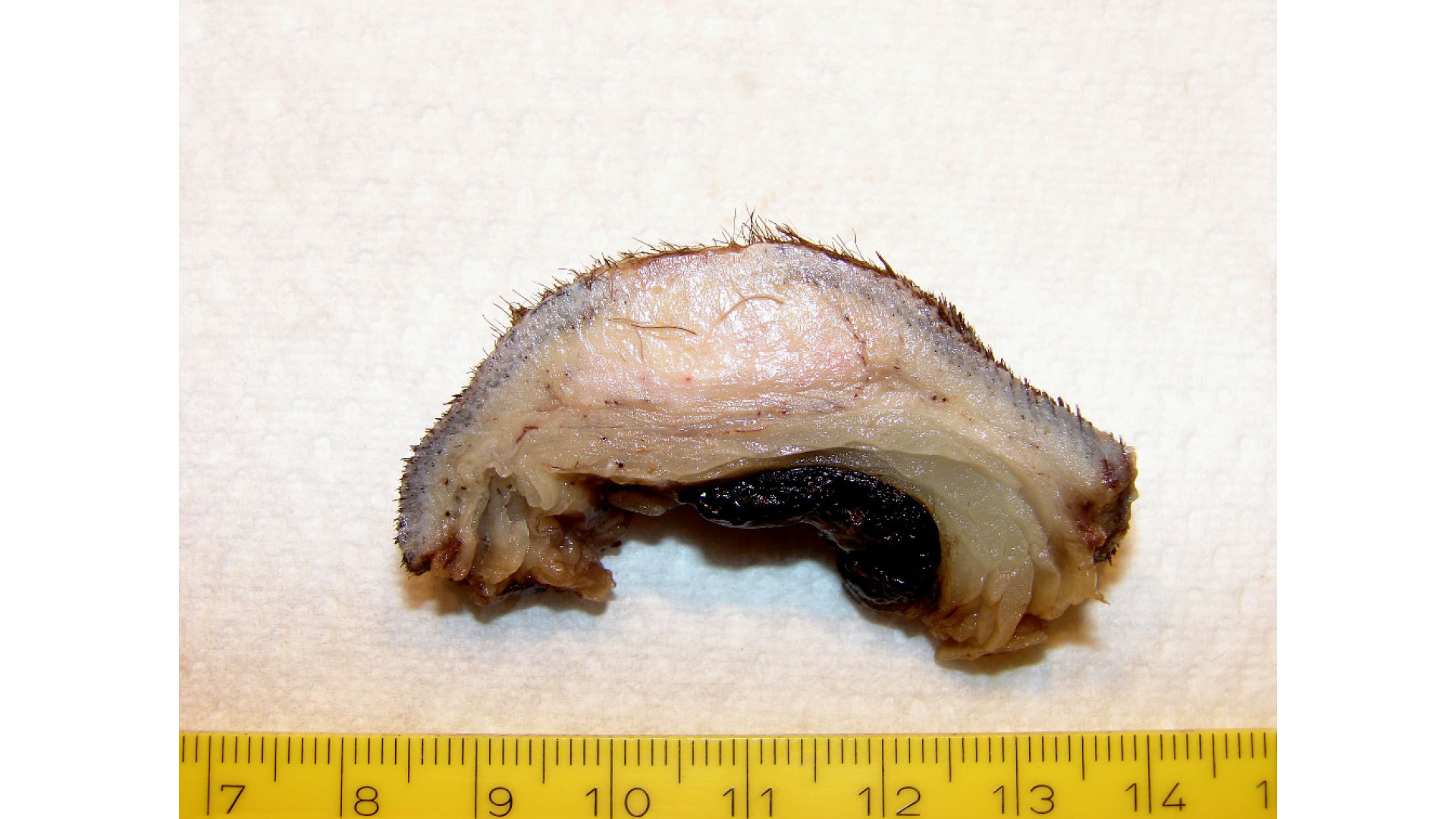
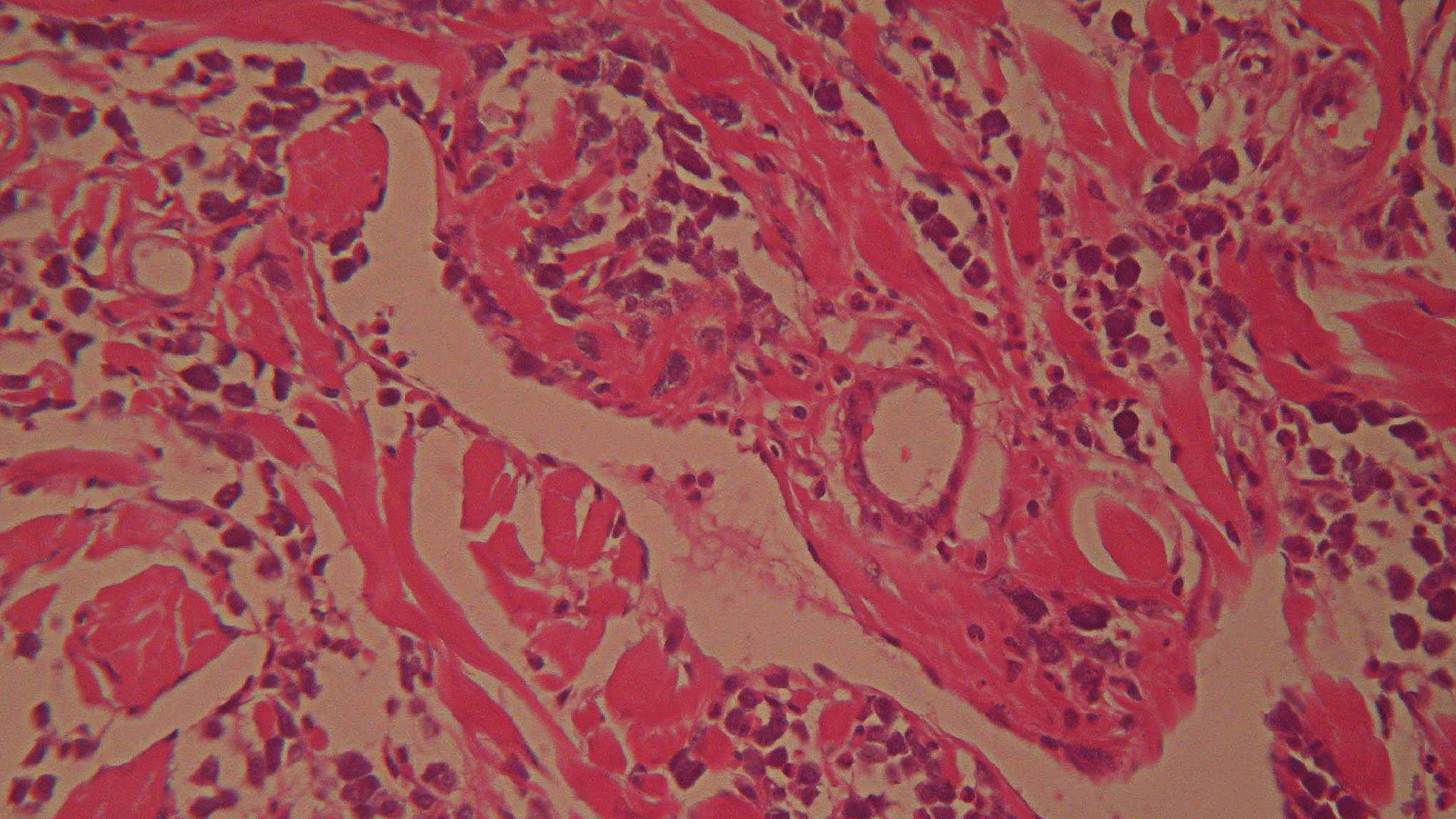
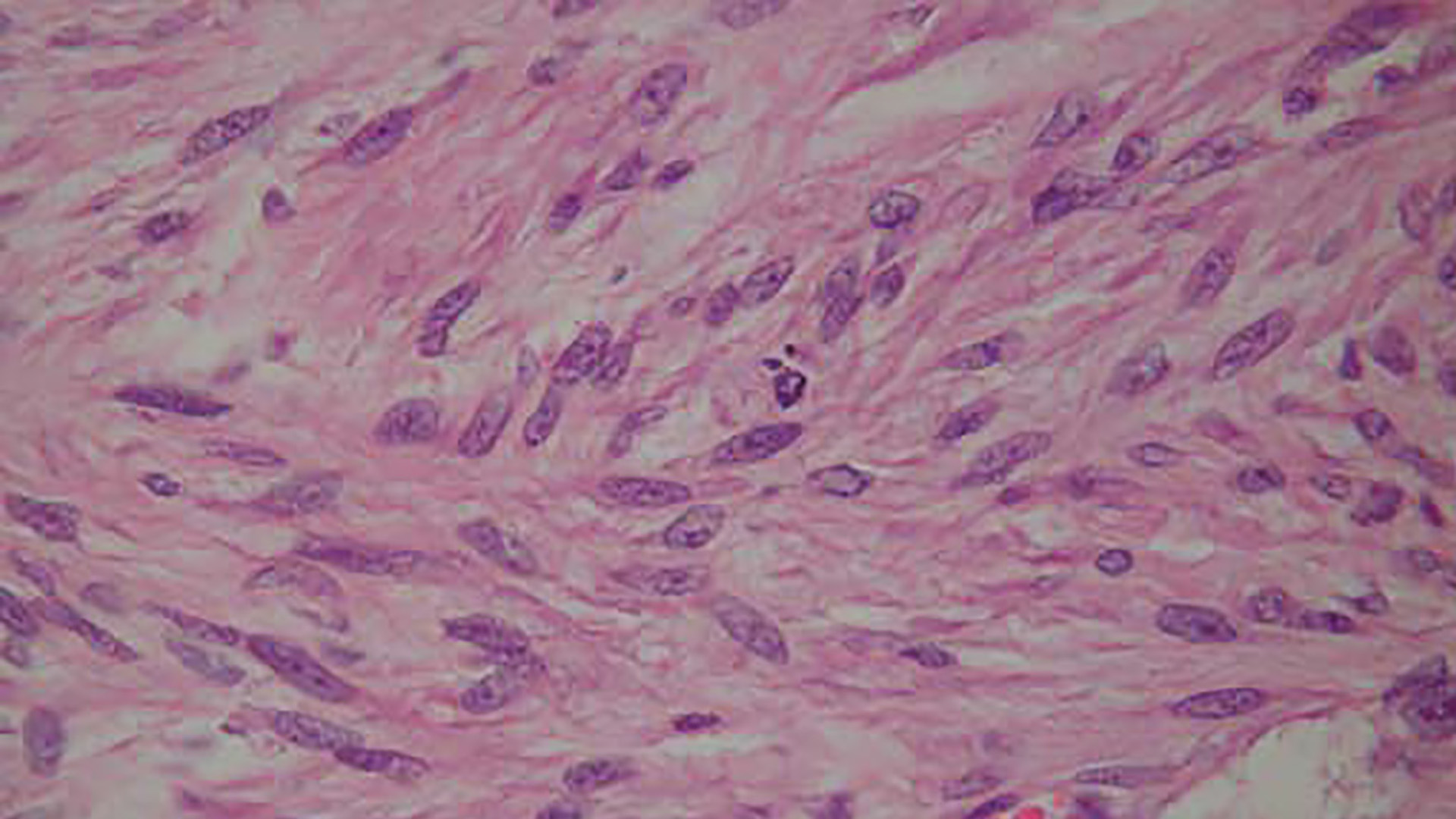
Das Problem besteht grundsätzlich darin, dass bei einem beschränkten Kostenrahmen nur eine begrenzte Anzahl von Gewebestückchen aus einer Probe untersucht werden kann (Abb. 1–3). Bei kleineren, gut begrenzten Tumoren von bis zu fünf Zentimeter Durchmesser kommt man mit einem bis drei untersuchten Gewebeteilen noch zu einem aussagekräftigen Ergebnis. Bei größeren, schlecht abgrenzbaren Tumoren wird eine solche Stichprobe allerdings recht klein, was sich zwar kaum in der Diagnosesicherheit, in hohem Ausmaß aber in der Aussagekraft bezüglich der Resektionsränder bemerkbar macht.
Es besteht in dieser Hinsicht ein großer Nachteil gegenüber bildgebenden Verfahren wie der -Computertomo-grafie oder der Magnetresonanztomografie, die ein Untersuchungsgebiet in nahezu beliebig vielen Schichten abtasten können. Dieser Nachteil kann nur teilweise durch eine deutlich höhere Anzahl von entnommenen Gewebeproben ausgeglichen werden. Manche Labors bieten diesen Service zu entsprechend höheren Kosten in Form einer Untersuchung von onkologischen Resektionsflächen an.
Außer der Stichprobengröße, die dem Tierarzt ja meist unbekannt bleibt, sind Breite und Gewebeart der Resektionsränder wichtige Parameter für die Beurteilung einer kompletten Resektion. Die Breite des tumorfreien umgebenden Gewebes sollte in Millimetern im Befund angegeben sein. Auch die Gewebeart ist von großer Bedeutung, da zum Beispiel das subkutane Fettgewebe weit weniger Hindernis für einen infiltrativ wachsenden Tumor darstellt als zum Beispiel eine Muskelschicht oder gar eine Faszie. Somit bieten zehn Millimeter Fettgewebe weit weniger Sicherheit für eine komplette Resektion als eine kaum einen Millimeter breite Faszie.
Fazit: Die Einschätzung der Rezidivneigung eines Tumors gründet sich immer auf die Tumorqualität sowie auf die Breite und die Art des umgebenden tumorfreien Gewebes und bezieht sich immer nur auf die untersuchten Schnitt-ebenen. Mehr Schnitt-ebenen bedeuten daher mehr Beurteilungssicherheit. Eine hundertprozentig sichere Aussage für den gesamten Tumor ist – abhängig von der Stichprobengröße –
nicht möglich. Je kleiner der Tumor, desto sicherer ist die Einschätzung der Rezidivneigung.