Ein Update zur Dirofilariose
beim Hund
Priv.-Doz. Dr. Michael Leschnik
Ausgabe 11/2019
Die mit Abstand häufigste Herzerkrankung des Hundes ist die chronisch degenerative Mitralklappenerkrankung.
Biologie und Verbreitung
Dirofilaria immitis ist der Erreger der kardiovaskulären Dirofilariose (Herzwurmerkrankung), während Dirofilaria repens die subkutane Dirofilariose verursacht. Als Endwirte werden vor allem Hunde und Wildkaniden beschrieben. Die weiblichen Würmer geben nach der Paarung Mikrofilarien (Larvenstadium 1) in den Blutkreislauf ab. Dort werden sie von Stechmücken beim Blutsaugakt aufgenommen. Nach der temperaturabhängigen Weiterentwicklung in der Mücke wird dort die Larve (Stadium 3) durch einen neuerlichen Stich in die Haut eines Säugetieres aktiviert und wandert dann aktiv in den Wirt ein. Im Unterhautbindegewebe häutet sich die Larve zum vierten und fünften Larvenstadium und wandert bei D. immitis in das rechte Herz und die Pulmonalarterien. Dort findet die Endreifung zur adulten Filarie statt, welche 15 bis 30 cm lang wird.
Bei D. repens erfolgen die letzte Häutung und die Vermehrung im subkutanen Bindegewebe des Wirtes. Diese adulten Würmer erreichen eine Länge von sieben bis 17 cm. Die Dauer von der Infektion bis zur Abgabe der Mikrofilarien in den Blutstrom (Präpatenz) wird beim Hund mit 26 bis 34 Wochen angegeben. Im Blutstrom überleben die circa 300 µm langen Mikrofilarien zwei bis18 Monate. Die Lebensdauer der Adulten wird mit bis zu 7,5 Jahre für D. immitis angegeben, D. repens überlebt im Wirt ebenfalls mehrere Jahre.
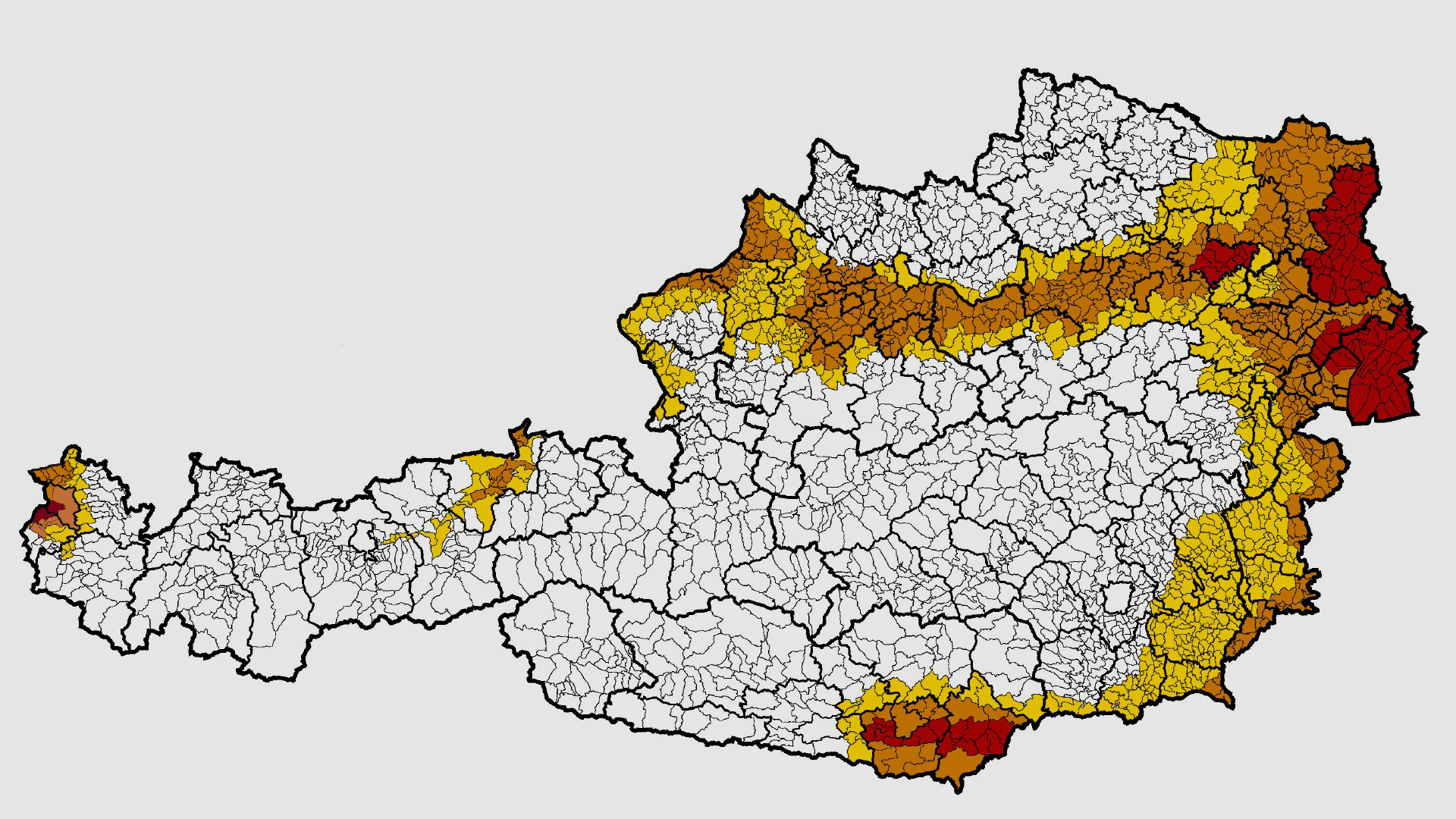
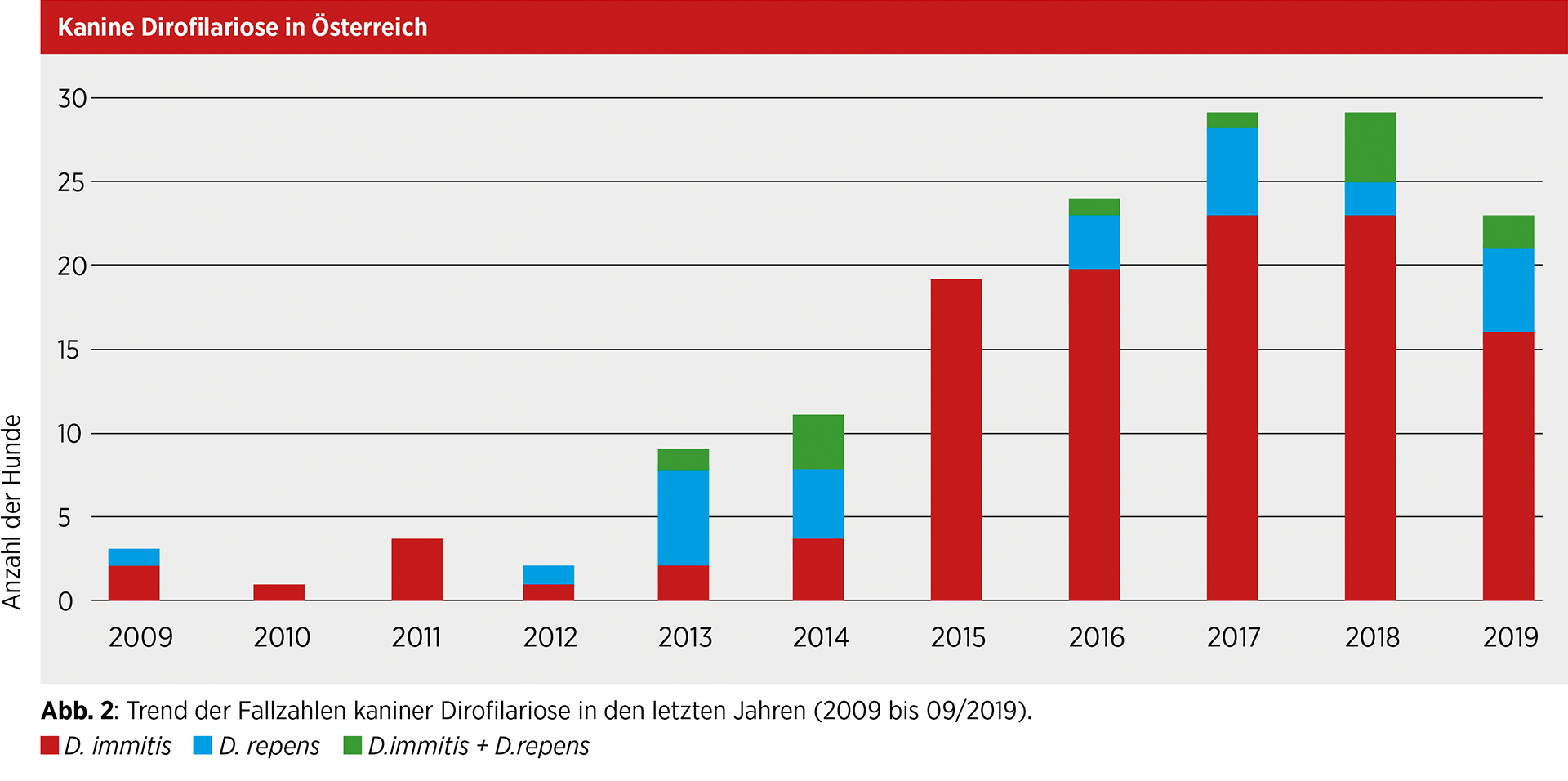
In Ostösterreich scheint die kutane Dirofilariose beim Hund bereits endemisch zu bestehen, da bereits einige Fälle ohne vorherigen Auslandsaufenthalt diagnostiziert wurden und D. repens auch in Stechmücken gefunden wurde. Ein erster Fall einer scheinbar autochthonen kardiopulmonalen Dirofilariose in Vorarlberg bestätigt den Verdacht, dass beide Erreger in Österreich bereits vorhanden sind bzw. die Endemisierung weiter voranschreitet. Eine aktualisierte Risikoanalyse ist in Abbildung 1 zu sehen und beruht auf Klimadaten und Falldaten beim Hund. Die steigenden Fallzahlen (Abb. 2) lassen sich durch verschiedene Aspekte erklären:
1) Deutliche Zunahme der Hundeimporte aus Ost- und Südosteuropa. Viele der importierten Tiere sind adult, was die Zeitspanne und damit die Wahrscheinlichkeit einer Infektion im Ausland verlängert bzw. erhöht.
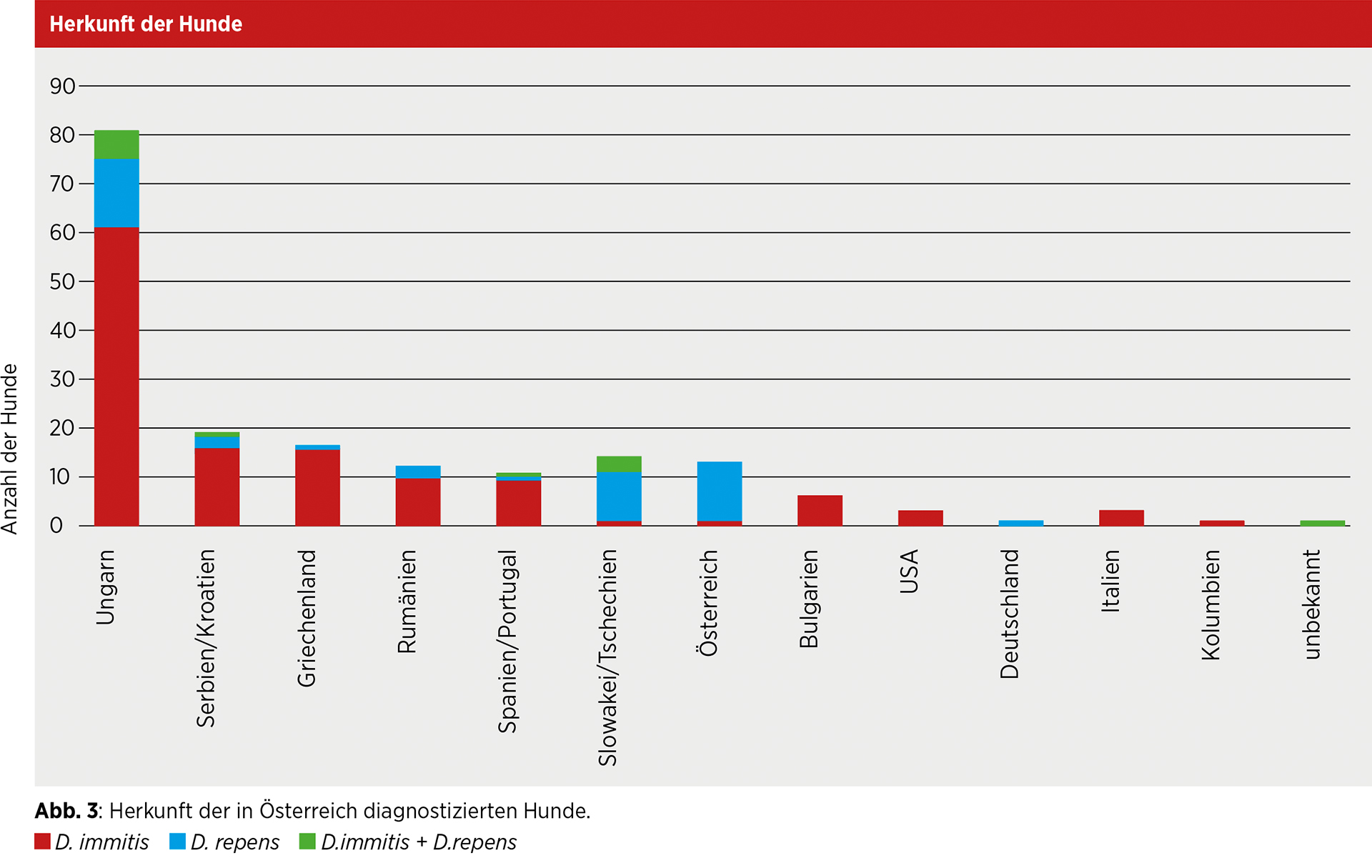
2) Ausbreitung der Endemiegebiete in Osteuropa: Hier zeigt sich v. a. in Ungarn, Serbien, Rumänien und Bulgarien eine massive Zunahme der Prävalenzen bei Hunden in Tierheimen von bis zu 70 Prozent (Abb. 3).
3) Zunehmende tierärztliche Initiative auf routinemäßiges Testen der importierten Hunde auf Reisekrankheiten und damit auch auf die Dirofilariose.
Pathogenese und Symptomatik
Infektionen mit D. immitis führen bei Hunden in unterschiedlichem Ausmaß zu klinischen Symptomen. Die adulten Nematoden im Bereich der Lungenarterien verursachen lokale Entzündungsreaktionen mit konsekutiver Verengung des Gefäßlumens und verminderter Elastizität der Blutgefäße. Daraus resultierende Symptome umfassen Leistungsintoleranz, Husten, Gewichtsverlust und nur in schweren Fällen mit hochgradigem Befall Symptome einer Rechtsherzinsuffizienz (Dyspnoe, Aszites) und pulmonalen Hypertension.
Bei hoher Parasitenbelastung oder beim plötzlichen Absterben von adulten Filarien kann es zur pulmonalen Thromboembolie (Lungeninfarkt) oder zum Vena-Cava-Syndrom mit zumeist letalem Ausgang kommen. Bei Tieren mit einem D.-immitis-Befall kann das klinische Erscheinungsbild in drei Stadien eingeteilt werden:
1. keine bzw. leichte Symptome wie seltener Husten und verminderte Leistungsbereitschaft;
2. chronischer Husten, Gewichts- und Konditions-verlust, Anstrengungsdyspnoe, geringgradige Anämie;
3. klinisch manifeste Herz- und Lungenveränderungen, Tachykardie und Tachypnoe, anämische Schleimhäute, systolischer Jugularvenenpuls, Hepatomegalie und Azotämie. Das Krankheitsbild kann auch perakut zum Schock und intravasaler Hämolyse führen.
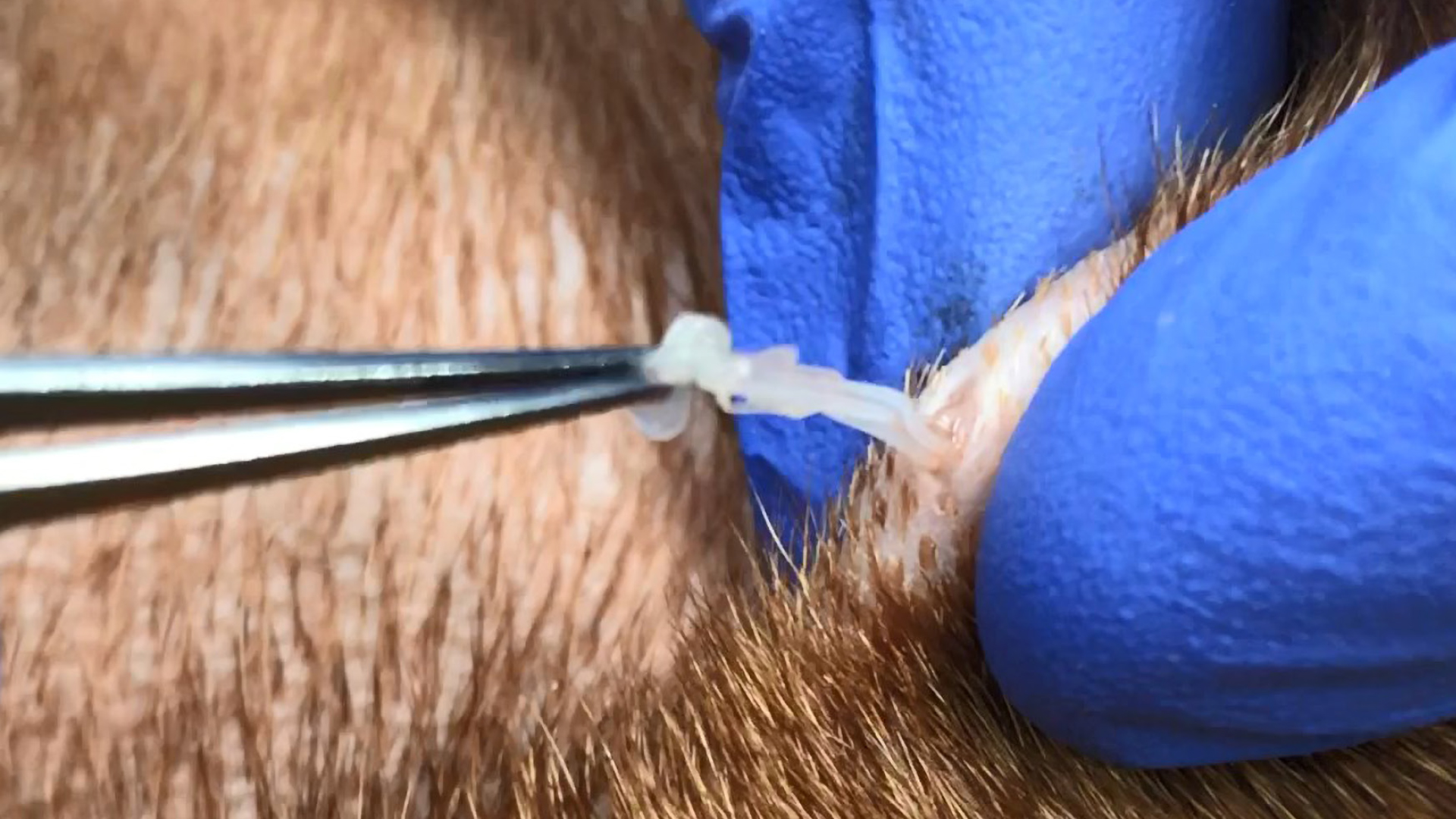
D. repens wird beim Hund zumeist zufällig bei der chirurgischen Eröffnung oder Entfernung von subkutanen Umfangsvermehrungen diagnostiziert oder bei einer ausgeprägten Mikrofilariämie im Blutausstrich oder seltener im Harn nachgewiesen.
Diagnose
Zur Diagnose der Herzwurmerkrankung beim Hund können sowohl die weiblichen adulten Filarien mit einem Antigennachweis (ELISA) als auch die Mikrofilarien (Knott-Test, PCR) aus EDTA-Blut nachgewiesen werden. Der Antigentest zeigt nur das Vorhandensein von geschlechtsreifen weiblichen adulten Filarien an und kann frühestens sechs bis acht Monate nach der Erstinfektion positiv ausfallen.
Somit ergibt sich die dringende Empfehlung bei importierten Hunden, diese nach der Ankunft in Österreich und ein zweites Mal sechs Monate später zu testen! Falsch negative Resultate liefert der Antigentest bei einem Befall mit ausschließlich männlichen Filarien und in der Phase der Präpatenz. Der Knott-Test kann bei fehlender Mikrofilariämie falsch negativ ausfallen.
Blutbildveränderungen sind generell unspezifisch. Mittels Thoraxröntgen kann der Schweregrad der Lungenveränderungen abgeschätzt werden, und im Herzultraschall können bei hoher Befallstärke Fadenwürmer im rechten Herz und im Anfangsteil der Pulmonalarterien visuell dargestellt werden. Eine Ultraschalluntersuchung von verdächtigen Hautknoten kann auch bei der subkutanen Dirofilariose die adulten Würmer darstellen.
Therapie und Prophylaxe
Die Prophylaxe der Dirofilariose wird mit larviziden Substanzen wie Moxidectin, Milbemycinoxim oder Selamectin durchgeführt. Die Anwendungen wirken auch im Sinne einer postexpositionellen Prophylaxe bei Infektionen, die bis zu 30 Tage vor Behandlungsbeginn erworben wurden. Zusätzlich können Repellentien zur Mückenabwehr eingesetzt werden. Die Therapie der Herzwurmerkrankung ist v. a. bei hochgradigem Befall mit Risiken für den Patienten verbunden. Das plötzliche Absterben vieler Makrofilarien kann einerseits zur mechanischen Obstruktion der Lungenarterien führen, andererseits eine überschießende Immunantwort mit allergischem Schock des Tieres bewirken. Prinzipiell sollten Hunde mit einer D.-immitis-Infektion bewegungsrestringiert werden, da ein transient erhöhter Blutdruck die Wahrscheinlichkeit von Thromboembolien erhöht. Als Adultizid wird Melarsamin eingesetzt.
Die Standardtherapie beinhaltet eine zweimalige intramuskuläre Injektion von jeweils 2,5 mg/kg in die Lumbalmuskulatur im Abstand von 24 Stunden mit einer Effizienz von 96 Prozent. Hierbei ist zumindest eine Sedierung des Patienten zu empfehlen, um die versehentliche Applikation in das Blutgefäßsystem zu vermeiden. Es hat sich gezeigt, dass die zusätzliche Therapie mit mikrofilariziden Substanzen und Doxycyclin sehr positive Effekte auf die Parasiteneliminierung hat, da dabei sowohl die Larven als auch die Endosymbionten (Wolbachien) der adulten Würmer und damit auch die Makrofilarien deutlich reduziert werden. Daraus ergeben sich zwei weitere Behandlungsschemata:
American Heartworm Society (AHS): Der Therapiestart erfolgt mit vier Wochen Doxycyclin oral (10 mg/kg bid). Daraufhin erfolgt eine einmalige Injektion von -Melarsamin, einen Monat später erfolgt die zweimalige Anwendung im Abstand von 24 Stunden. Es wird monatlich ein mikrofilarizides Medikament verabreicht. Die Effizienz erreicht hier bis zu 100 Prozent nach sechs Monaten. Prednisolon (0,5 mg/kg zweimal täglich oral über ein bis zwei Wochen ausschleichend) sollte nur nach klinischer Indikation zur Reduktion einer Bronchopneumonie und bei Reaktionen auf die adultizide Therapie verabreicht werden. Behandlungsschema nach Leschnik (bei asymptomatischem D.immitis-Befall oder milder Symptomatik): Doxycyclin wird für drei Wochen verabreicht und monatlich das Mikrofilarizid. Nach drei Wochen wird eine zweimalige Melarsamin-Injektion im Abstand von drei Tagen appliziert. Nach sechs Monaten werden die Bluttestkontrollen durchgeführt. Zu diesem Zeitpunkt zeigt sich eine Effizienz der Therapie von 93,5 Prozent.
Sofern der Antigentest noch immer schwach positiv ist, kann mit einer einmaligen Melarsamin-Injektion die Therapie erfolgreich beendet werden oder mit der weiteren monatlichen Gabe eines makrozyklischen Laktons auf ein „Slow-kill“-Protokoll umgestiegen werden.
Das Slow-kill-Protokoll beinhaltet ebenfalls ein Doxycyclin zu Beginn und danach die monatliche Gabe des makrozyklischen Laktons. Hierbei sind die Behandlungskosten zwar niedriger, aber die Therapiedauer verlängert sich in den meisten Fällen auf über ein Jahr, weshalb die AHS dieses Protokoll nicht empfiehlt. Bei einem Befall mit D. repens sollten die adulten Würmer in der Unterhaut chirurgisch entfernt werden. Die Therapie mit Moxidectin über sechs Monate ist zur Behandlung der subkutanen Dirofilariose zugelassen.
Zoonoseaspekt
Beim Menschen entwickeln sich Dirofilarien zumeist nicht bis zum Adultstadium, und es kommt daher nur in wenigen Fällen zur Mikrofilariämie. Subkutane, okuläre oder pulmonale Granulome wurden beschrieben und fälschlicherweise immer wieder als Neoplasien klassifiziert. Menschen sind von der Prävalenz in der lokalen Hundepopulation direkt betroffen, da zwar eine direkte Übertragung vom Hund auf den Menschen ausgeschlossen ist, aber positive unbehandelte Hunde die Erregerprävalenz in der lokalen Stechmückenpopulation so erhöhen, dass auch Personen häufiger infiziert werden.
Literaturliste
Bazzocchi C., Mortarino M., Grandi G., Kramer L. H., Genchi C., Bandi C., Genchi M., Sacchi L., McCall J. W. (2008): Combined ivermectin and doxycycline treatment has microfilaricidal and adulticidal activity against Dirofilaria immitis in experimentally infected dogs. Int. J. Parasitol. 38: 1401–1410.
Duscher G., Feiler A., Wille-Piazzai W., Bakonyi T., Leschnik M., Miterpáková M., Kolodziejek J., Nowotny N., Joachim A. (2009): Detection of Dirofilaria in Austrian Dogs. Berl. Munch. Tierärztl. Wochenschr. 122: 199–203.Genchi C., Venco L., Genchi M. (2007): Guideline for the laboratory diagnosis of canine and feline Dirofilaria infections. In: C. Genchi, Rinaldi L. and Cringoli G. (Hrsg.) Naples, Italy: Veterinary Parasitologyand Parasitic Diseases., 137–144.
Hinney B. und M. Leschnik (2015): Reiseparasitosen der Hunde und Katzen. Kleintierpraxis 60, 254–282.
Leschnik M., Löwenstein M., Edelhofer R., Kirtz G. (2008): Imported non-endemic, arthropod-borne and parasitic infectious diseases in Austrian dogs. Wien. Klin. Wochenschr. 120: 59–62.
American Heartworm Society Guidelines: https://d3ft8sckhnqim2.cloudfront.net/images/documents/Canine_Guidelines_Summary_German.pdf?1503892936
