Multiresistente Pseudomonas-aeruginosa-Infektion
Management der Infektion in der Kleintierpraxis
Dr. Antje Wolf
Tierklinik Schwarzmann
Ausgabe 09/2020

Pseudomonas aeruginosa zählt weltweit zu den häufigsten Ursachen von nosokomialen Infektionen. Der vorliegende Fallbericht beschreibt den Verlauf einer positiven Behandlung.
Infektionen mit multiresistenten Keimen stellen den Tierarzt in der Praxis immer häufiger vor große therapeutische Herausforderungen. Der folgende Bericht beschreibt den Fall einer fünfjährigen Jagdhündin, die infolge einer Infektion mit einem multiresistenten Pseudomonas aeruginosa und einer daraus folgenden schwerwiegenden Hautläsion in der Klinik vorgestellt wurde.
Anamnese
Eine fünfjährige Deutsch-Kurzhaar-Hündin wurde aufgrund einer nicht heilenden Verletzung im Bereich des rechten Carpus vorgestellt. Die Hündin ist intakt, wiegt 34 Kilo, wird viermal jährlich entwurmt und jährlich geimpft, stammt aus einer sächsischen Zucht und wurde jagdlich geführt. Zwei Wochen zuvor hatte sich die Hündin im Wald ein Trauma im Bereich des linken Carpus zugezogen; dies war chirurgisch vom Haustierarzt versorgt worden. Zusätzlich wurde ein Gyrasehemmer für zehn Tage und ein unbekanntes NSAID für fünf Tage verordnet. Die Wunde wurde mit einem Verband versorgt. Die Hündin konnte das Bein nicht belasten, beim ersten Verbandswechsel nach drei Tagen war das gesamte Bein warm und geschwollen, die chirurgische Wundnaht zum Teil gelöst bzw. ausgerissen. Daraufhin wurde die Wunde noch einmal eröffnet, gespült und eine zusätzliche Antibiose mit Cefalexin gestartet. Innerhalb der nächsten Tage begann die Wunde zu eitern und es bildeten sich ein immer größer werdendes Wundbett sowie ein unangenehmer Geruch der Wunde. Da sich die Hündin zusehends schmerzhafter zeigte, wurde sie auf Wunsch der Halter in der Klinik vorgestellt.
Klinische Befunde
Die Hündin war während der Untersuchung ruhig, zeigte jedoch beim Lösen des Verbands Schmerzen. Die klinische Untersuchung ergab eine innere Körpertemperatur von 38,5 °C, eine Atemfrequenz von 32 Atemzügen pro Minute und eine Pulsfrequenz von 100 Schlägen pro Minute. Die Schleimhäute waren rosa, die kapilläre Füllungszeit betrug < 2 s. Es lagen keine Abweichungen von der klinischen Norm vor. Die linken Vordergliedmaßen waren im Bereich des Carpus wärmer als der übrige Hund, im Bereich des Traumas deutlich heißer. Die Wunde verlief nahezu zirkulär karpal über eine Fläche von 10 × 4 cm. Fibrinauflagerungen, gemischt mit eitrigem Wundsekret, an den Rändern mit partiell nekrotischen Arealen und einem hefig-modrigen Geruch vervollständigten das Wundbild. Unter den Wunddefekten lagen zum Teil Sehnen und Knochenstrukturen frei.
Diagnostische Verfahren
Es wurden eine hämatologische und biochemische Blutuntersuchung und ein Röntgenbild des betroffenen Beins angefertigt.
Blutuntersuchung
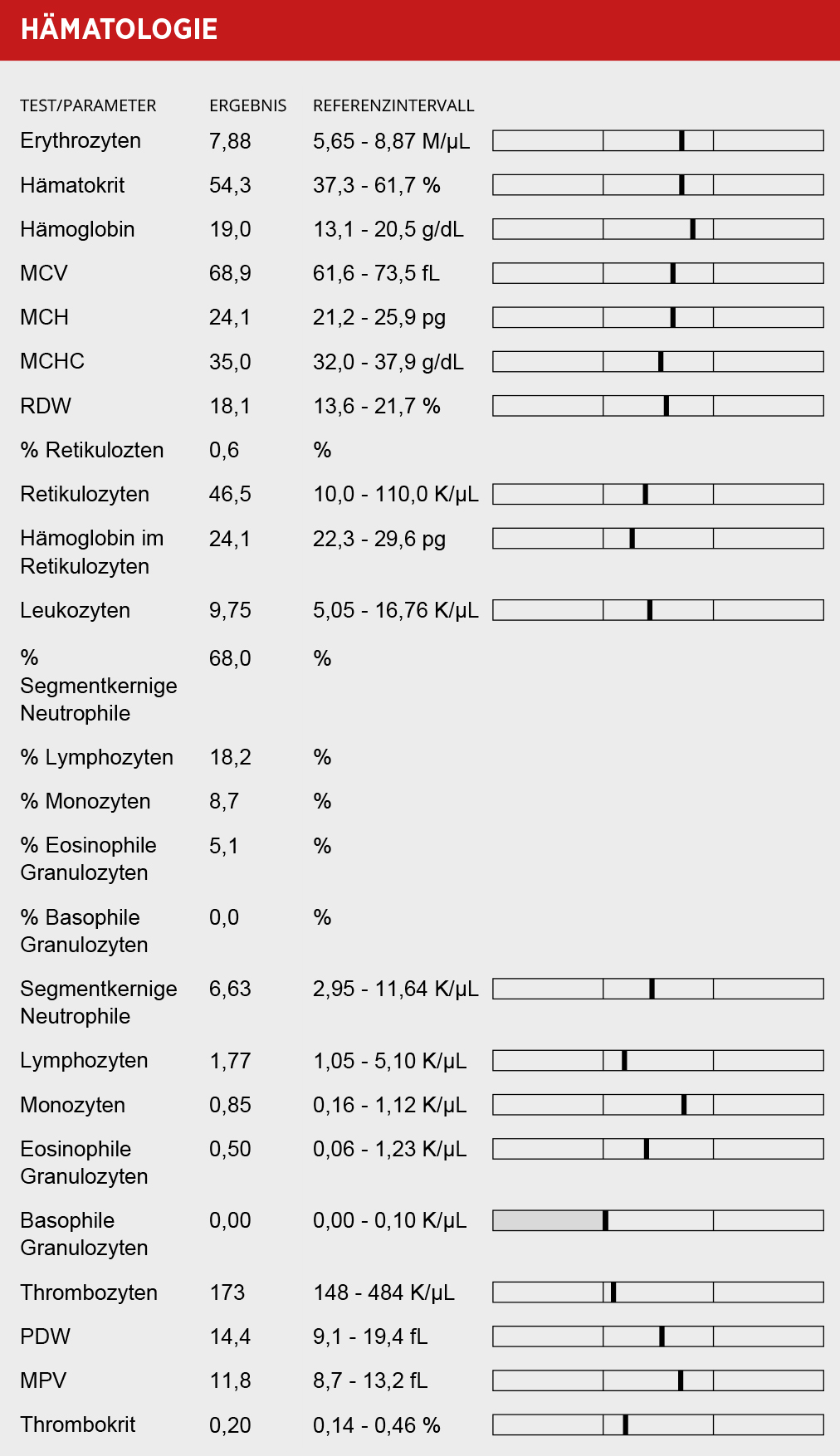
Die Hündin erhielt einen peripheren Venenkatheter in die Vena cephalica des linken Vorderbeins. Darüber nahm man der Hündin Blut zur Untersuchung (Differenzialblutbild im „Procyte“, Blutchemie im „Catalyst Dx“; Tabelle 1) ab.
Der Befund ergab eine erhöhte CRP-Konzentration, sonst keine Abweichungen abseits der Norm.
Orthopädische Untersuchung
Die orthopädische Untersuchung des betroffenen Carpus zeigte keine Veränderungen abseits der Norm.
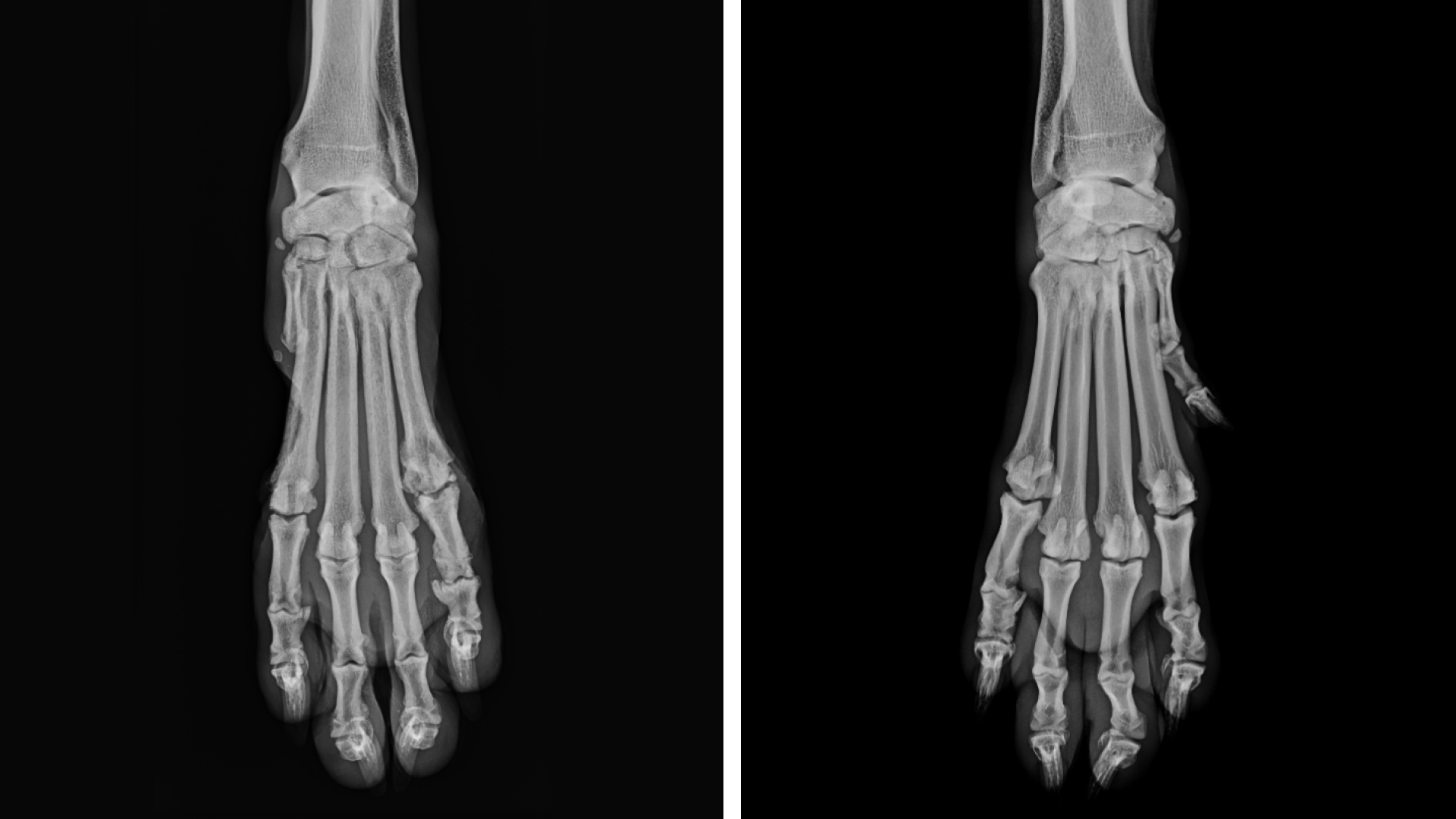
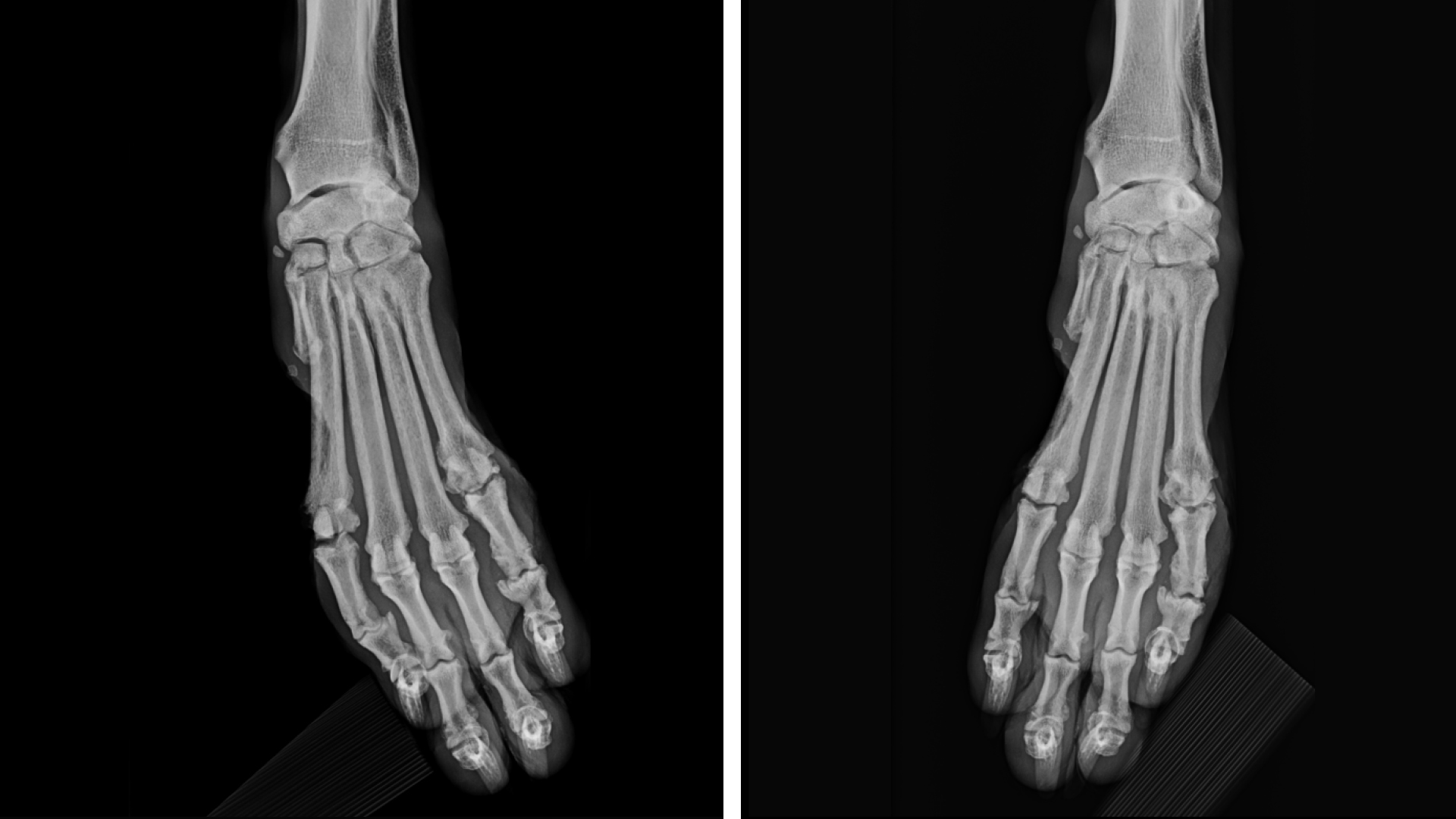
Röntgen
Das Röntgenbild des betroffenen Carpus ergab keine Veränderungen an den knöchernen Strukturen (Abbildung 1) abseits der Norm, zudem wurden „Stressröntgen“ in Flexion und Extension angefertigt, die ebenso keine Abweichung abseits der Norm ergaben.
Zytologie der Wunde
Schleimig-schlieriges Material, Granulozyten, Erythrozyten, massenhaft Stäbchenbakterien (Abbildung 2).
Vorläufige Arbeitsdiagnose
Infiziertes Weichteiltrauma im Bereich des linken Carpus.
Weitere Diagnostik und Therapie
Die Hündin wurde stationär aufgenommen und am gleichen Tag ein Wunddebridement mit Probenentnahme zur bakteriologischen Untersuchung sowie Antibiogramm entnommen. Während des stationären Aufenthalts und des chirurgischen Eingriffs erhielt die Hündin eine intravenöse Dauertropfinfusion mit isotoner Kristalloidlösung (Ringer-lactat, Braun) mit einer Infusionsrate von 4 ml/kg KGW/ h). Zur Einleitung der Narkose wurde Methadon HCL (0,5 ml/kg KGW i. v.) plus Acepromazin (0,2 mg/kg KGW i. v.) und Ketamin (10 mg/kg KGW i. v.) gewählt und anschließend die Anästhesie in Isofluran (1,5 %) weitergeführt. Die Tupferproben wurden entnommen, bei der Wundrevision war zu sehen, dass das Os metacarpale III aufgrund des Weichteiltraumas zum Teil frei liegend war, wobei der Ansatz des M. extensor carpi radialis zwar ebenso partiell frei liegend, jedoch nicht verletzt war.
Im Rahmen des Wunddebridements wurden die schleimig-schlierigen Auflagerungen und das nekrotische Material entfernt, die Wunde intraoperativ großzügig mit steriler isotoner Kochsalzlösung (NaCl Braun) gespült. Im Anschluss daran folgten eine Spülung mit TrisNAC (ICF, Prozoon) und Versorgung der Wunde mit einem Pfoten bzw. durchgehenden Stützverband über die Länge der ganzen Gliedmaße zur Ruhigstellung. Zur Wundauflage wurde eine Tielle Silicone Border verwendet, eine nicht haftende, aber gut saugende Wundauflage. Die Hündin wurde noch am gleichen Tag in die häusliche Pflege entlassen. Um die Zeit bis zum Befund der bakteriologischen Untersuchung zu überbrücken, wurde der Verband täglich gewechselt bzw. die Wunde täglich mit TrisNAC gespült und die Wundauflagen erneuert. Zusätzlich erhielt die Hündin einmal täglich 4 mg/kg Carprofen (Rimadyl).
UntersuchungsErgebnis und weiterer Verlauf
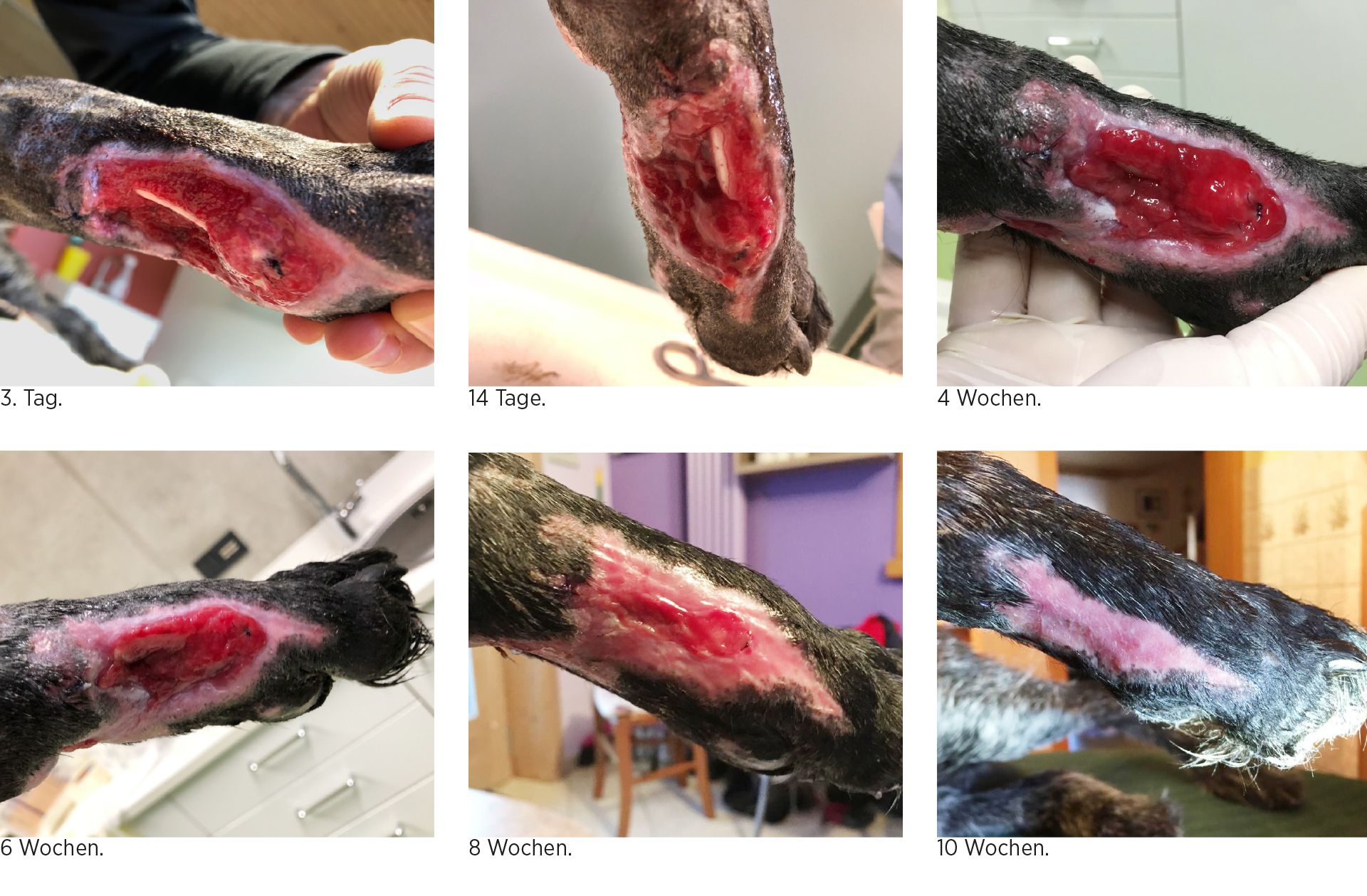
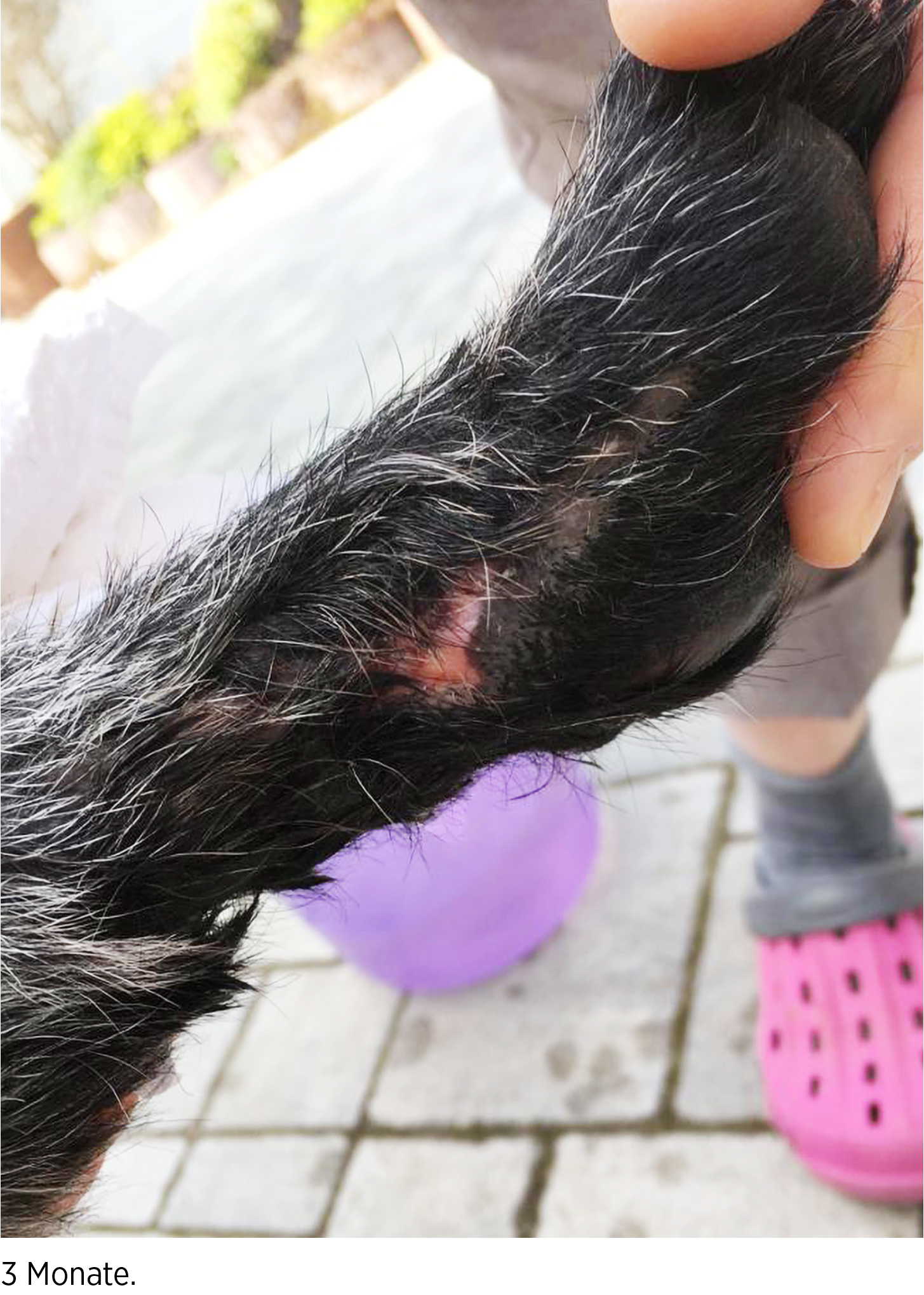
Die bakteriologische Untersuchung befundete eine multi-resistente Pseudomonas-Bakterien. Die Hündin befand sich zu diesem Zeitpunkt an Tag sechs der gestarteten Wund- und Verbandstherapie, die weiter gute Fortschritte zeigte. So wurde gemeinsam mit dem Halter besprochen, die täglichen Wundpflegen und Verbandswechsel ambulant weiterzuführen. Aufgrund des Antibiogramms hätte auf ein Reserveantibiotikum zurückgegriffen werden müssen, dies wäre aber in Anbetracht der potenziellen Nebenwirkungen gegenüber dem Therapiefortschritt zu diesem Zeitpunkt nicht zu empfehlen gewesen. Auf den nebenstehenden Bildern (links) sind die Fortschritte der Wundheilung jeweils im wöchentlichen Abstand zu sehen. Im Folgenden wurden die Läsionen nach der Wundtoilette täglich mit TrisNAC gespült und eine frische Tielle Silicone Border aufgelegt. Die schleimig-schlierigen Auflage-rungen auf der Wunde ließen innerhalb der ersten drei Tage der Behandlung deutlich nach. Bis zur bakteriologischen Befundung und dem Antibiogramm vergingen insgesamt sechs Tage. Innerhalb von 48 Stunden begann die Bildung von saftigem, tiefrotem Granulationsgewebe, die Schmerzhaftigkeit ließ spürbar nach, zudem die Schwellung im Bereich des Carpus.
Die Wundheilung ging mit der Etablierung von saftig--rotem Granulationsgewebe zügig weiter, nach insgesamt acht Wochen gelang der Wundschluss. Der Wechsel vom Stützverband auf einen Schutzverband fand nach drei -Wochen statt. Rimadyl wurde insgesamt 14 Tage verabreicht. Die Hündin wurde über die ganze Zeit der Wundheilung lediglich für mehrmals täglich 15 Minuten an der Leine Gassi geführt.
Diskussion
Pseudomonas aeruginosa zählt weltweit zu den häufigsten Ursachen von nosokomialen Infektionen. Das natürliche Reservoir für diesen Keim sind Feuchtbiotope, wobei er auch in Feuchtbereichen von Kliniken zu finden ist. Patienten infizieren sich am häufigsten durch Kontakt mit dem Erreger in der Umwelt sowie in Kliniken von Patient zu Patient. Die meisten P.-aeruginosa-Stämme sind von Natur aus gegen eine Vielzahl von Antibiotika resistent. Auch in der Veterinärmedizin stellen zunehmende Resistenzentwicklungen von Bakterien gegen antibiotische Substanzen ein Problem in der täglichen Praxis dar.
Dabei spielt die Produktion des Biofilms eine wichtige Rolle. Dieser Biofilm, eine Gemeinschaft aus DNA, Polysacchariden und Proteinen, schützt die darin eingebetteten Bakterien vor dem Immunsystem und macht sie so unempfindlicher gegen Antibiotika.
Dies stellt den Praktiker bei der Therapie zudem vor die Herausforderung, dass gerade lokal applizierte Antibiotika die Bakterien nur in geringer Konzentration erreichen, die nicht ausreicht, um sie abzutöten. Die Folge ist, dass höhere Konzentrationen durch Dosiserhöhung des Antibiotikums notwendig sind, um die minimale Hemmstoffkonzentration und die minimale bakterizide Konzentration zu erreichen. Dies wiederum zieht das Risiko nicht unerheblicher Nebenwirkungen nach sich.
Die Zerstörung des Biofilms stellt einen neueren Therapie-ansatz in der Behandlung von multiresistenten bakteriellen Infektionen dar. TrisNAC ist eine Lösung aus TrisEDTA und Natrium-Acetylcystein (NAC). NAC hat eine mukolytische Komponente und ist zudem antimikrobiell. TrisNAC ist eine neuartige und synergistische Verbindung von NAC und Tris-EDTA und wird als wirksame Unterstützung verabreicht, um die Ausbildung eines bakteriellen Biofilms zu verhindern. TrisEDTA führt zu einer physikalischen Zerstörung der Bakterienwände und wirkt synergistisch mit NAC in der Zerstörung des Biofilms. Dadurch steigert TrisNAC die Wirksamkeit von antimikrobiellen Substanzen. Der Tielle-Silicone-Border-Hydropolymerverband mit Silikon absorbiert Exsudat, hält ein feuchtes Wundheilungs-milieu und minimiert das Mazerationsrisiko. Dabei spielt die Kombination aus Absorptionsvermögen und Dampfdurchlässigkeit eine entscheidende Rolle. Der Verband besteht aus einer verklebenden Wundkontaktschicht aus perforiertem, weichem Silikongel, einem saugfähigen Wundkissen aus Hydropolymerschaum, einer stark absorbierenden Vliesschicht und einem hochgradig atmungs-aktiven Filmträger. Der Filmträger ist wasserdicht und wirkt als bakterielle Barriere.
Die Therapie von Infektionen mit multiresistenten Keimen stellt für den Praktiker der Veterinärmedizin immer häufiger hinsichtlich der biologischen Eigenschaften des Keims, des Allgemeinzustandes des Patienten, der Art und Lokalisation der Infektion und der zur Verfügung stehenden therapeutischen Möglichkeiten eine Herausforderung dar. Dabei haben die möglichen Nebenwirkungen der potenziell sensiblen Antibiotika sicherlich einen -genauso großen Stellenwert wie die Verantwortung, dass in der -veterinärmedizinischen Praxis teilweise Reserveantibiotika für die Humanmedizin verwendet werden.
Zusammenfassend führen diese Überlegungen zu dem Schluss, dass für jeden Patienten mit einer derartigen Infektion ein individueller Therapieplan zu erstellen ist. Dabei ist die Zerstörung des Biofilms ein neuartiger Therapieansatz, der uns neue Wege in der Therapie von multiresistenten Infektionen weist.
Im vorliegenden Fall wurde die Therapie nach dem Wunddebridement mit einer lokalen Wundpflege bzw. -spülung weitergeführt. Hierbei war augenscheinlich, wie sehr die Heilung der Wunde von der täglichen großzügigen Reinigung und Behandlung mit TrisNAC profitiert hat.
Die Wahl fiel auf den Tielle-Wundschutz, da dieser eine sehr gute Wundflüssigkeitsaufnahme bei gleichzeitiger Instandhaltung des Granulationsgewebes bietet. Die zusätzliche Ruhigstellung der Gliedmaße stellt einen -unterstützenden Faktor für die möglichst ungestörte Wundheilung dar.
Quellen
Robert-Koch-Institut: Antibiotikaresistenz -Pseudomonas aerugino-sa, www.rki.de (2017).
Helmholtz-Zentrum für Infektionsforschung: Bakterielle Biofilme detektieren und bekämpfen (2017).
Tim Nuttall, Lynette K. Cole: Evidence-based Veterinary dermatology: a systematic review of interventions for treatment of Pseudomonas otitis in dogs. Veterinary Dermatology 18 (2), 6977.
R. Roy, M. Tiwari, G. Donelli, V. Tiwari: Strategies for combating bacterial biofilms: A focus on anti-biofilm agent and their mechanisms of action. Virulence 2018, 9 (1): 522–554.
Charlotte C. Pie, Anthony A. Yu, J. Scott Weese: Evaluation of biofilm production by Pseudomonas aeruginosa and the impact of biofilm on antimicrobial susceptibility in vitro. Veterinary dermatology (2013) 24 (4).
C. E. Griffin: Diagnosis and management of chronic otitis externes and media with multiresistent bacteria. 18. Jahrestagung der DGVD (2017) 113–115.
S. Peters. Livisto: Thema: Die Lösung gegen Biofilm (2018).
Fachinformation AcelityTM. Systagenix Wound Management Limited, Gargrave, North Yorkshire, BD23 3RX, UK (2016).
