Wann ist eine Bestrahlungstherapie indiziert?
Eine Bestrahlungstherapie ist indiziert für maligne Tumoren, die entweder nicht ausreichend weit chirurgisch reseziert werden können, oder bei denen gar keine chirurgische Resektion möglich ist. Vor jeder Bestrahlungstherapie müssen die Tumordiagnose, das vorliegende Krankheitsstadium und eventuell vorliegende Begleit-erkrankungen bekannt sein. Diese diagnostische Aufarbeitung des Patienten (= Staging) kann entweder bereits durch den zuweisenden Tierarzt oder auch durch das Onkologieservice der Vetmeduni Vienna durchgeführt werden. Je nach Ergebnis dieses Tumorstagings kann eine Bestrahlung kurativ oder palliativ angewendet werden. Ziel einer kurativen Bestrahlung ist eine langfristige lokale Tumorkontrolle. Bestrahlungsprotokolle sind daher aggressiver ausgerichtet und verwenden eine hohe Gesamtdosis (ca. 45 bis 52 Gray). Einzelfraktionen von ca. drei Gray (Gy) werden typischerweise täglich (fünfmal pro Woche) über einen Zeitraum von etwa 3,5 Wochen in 15 bis 16 Einzelfraktionen verabreicht. Eine möglichst geringe Einzelfraktionsdosis minimiert das Risiko von unerwünschten chronischen Nebenwirkungen. Eine palliative Bestrahlung ist hingegen nicht auf eine Langzeitkontrolle des Tumors ausgerichtet, sondern auf eine Erhaltung bzw. Verbesserung der Lebensqualität und eine kurzfristige Tumorkontrolle. Daher wird eine palliative Bestrahlung typischerweise bei Vorliegen fortgeschrittener Krankheitsstadien oder therapiebeeinflussender Begleiterkrankungen eingesetzt. Palliative Protokolle sind weniger aggressiv und verwenden niedrigere Gesamtdosen (20 bis 36 Gy) als kurative Protokolle. Weiters besteht eine Behandlung aus wenigen Einzelfraktionen (meist drei bis sechs Fraktionen), die entweder täglich oder ein- bis zweimal pro Woche verabreicht werden. Die Einzeldosis selbst ist höher als bei kurativen Protokollen – bei täglichen Protokollen sind es meist vier Gy, bei ein- bis zweiwöchentlichen Behandlungen liegt diese bei acht Gy oder sechs Gy. Typische Beispiele für Tumoren, die häufig palliativ bestrahlt werden, sind kanine appendikuläre Osteosarkome oder feline Plattenepithelkarzinome der Maulhöhle.
Soll eine Behandlung in Kombination mit einem chirurgischen Eingriff durchgeführt werden, muss überlegt werden, ob prä- oder postoperativ bestrahlt werden soll. Typische Indikationen für einen kombinierten Einsatz mit einer chirurgischen Intervention sind:
• Eine großzügige Tumorexzision ist nicht möglich,
• der histologische Schnittrand weist Tumorzellen auf bzw. weist einen zu knappen tumorfreien Rand auf (bei Erstellung des Therapieplans sollte allerdings bereits realistisch abgeschätzt werden, ob eine saubere Resektion möglich ist),
• der Besitzer lehnt eine aggressive Chirurgie‚ (z. B. Amputation) ab.
Tumore, die häufig in Kombination mit einer chirurgischen Resektion bestrahlt werden, sind Tumore der Maulhöhle und Weichteilsarkome oder Mastzelltumore der Haut- und Unterhaut, insbesondere an den distalen Extremitäten.
Bestrahlung ohne chirurgischen Eingriff wird bei Tumoren angewendet, bei denen eine chirurgische Intervention nicht oder nur bei hohem Risiko möglich ist bzw. der Besitzer einen chirurgischen Eingriff ablehnt. Voraussetzung für eine alleinige kurative Bestrahlung ist ein strahlensensitiver und nicht zu großer Tumor. Beispiele für Tumoren, die alleine kurativ bestrahlt werden können, sind Gehirntumore, fixierte Schilddrüsentumore, Ameloblastome der Maulhöhle oder Thymome. Weiters wird eine alleinige Bestrahlung häufig in palliativer Form für inoperable und für eine kurative Therapie zu weit fortgeschrittene Tumoren eingesetzt.
Da eine Strahlentherapie i. R. als lokale Therapieform eingesetzt wird, ersetzt sie bei Tumoren mit hohem Metastasierungsrisiko nicht eine Chemotherapie oder eine andere systemische Therapie. Es bleiben in diesen Fällen immer einerseits der Problemkreis „Primärtumor“ und andererseits der Problemkreis „Metastasen“ zu berücksichtigen. Sehr wohl wird eine Bestrahlung zur Behandlung regionaler Lymphknotenmetastasen eingesetzt. Dies ist also bei Tumoren relevant, die über die Lymphbahn streuen, wie beispielsweise Mastzelltumore oder auch orale Melanome.
Welches Strahlentherapiegerät steht an der VetMedUni Vienna zur Verfügung?
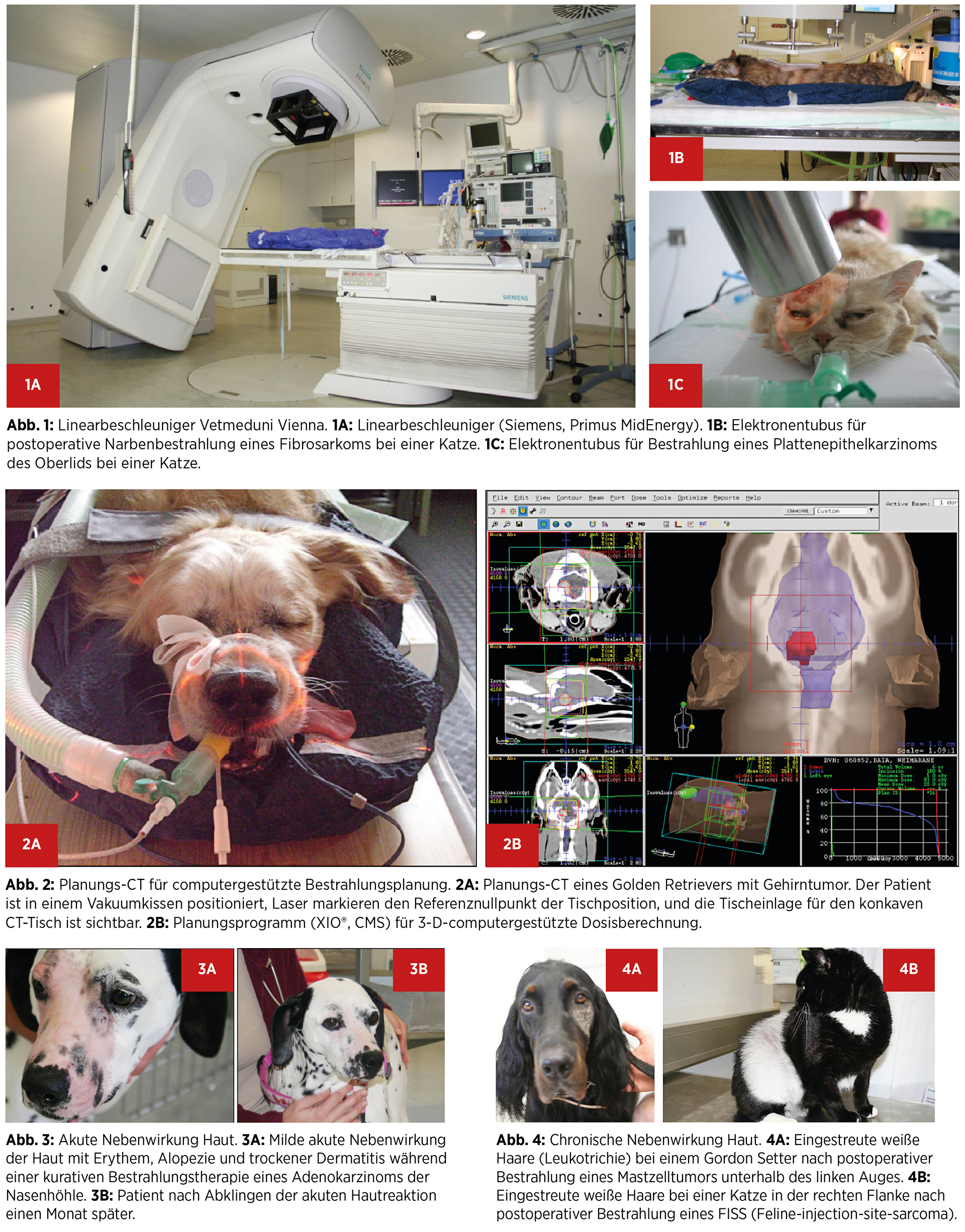
An der Vetmeduni Vienna wird ein sogenannter Linearbeschleuniger zur Behandlung von onkologischen Kleintierpatienten eingesetzt (Siemens Primus MidEnergy, Abb. 1A). Ein solches Gerät produziert hochenergetische Röntgenstrahlung (sechs MV-Photonen) durch Beschleunigung von Elektronen in einem hochfrequenten elektromagnetischen Feld. Diese Elektronen können auch direkt für eine Behandlung genutzt werden (Wahl fünf bis 14 MeV). Linear-beschleuniger verwenden große Fokus-Haut-Abstände (100 cm) und erlauben eine isozentrische Drehung des Bestrahlerkopfes um den Patiententisch. Dadurch kann der Patient aus verschiedenen Richtungen ohne Umlagerung bestrahlt werden. Der Grund, warum in der Strahlentherapie überwiegend Linearbeschleuniger eingesetzt werden, liegt darin, dass bei einer Photonenenergie W> 1 Megavolt (MV) der fotoelektrische Effekt keine -Rolle mehr spielt, die Interaktion mit dem absorbierenden Gewebe erfolgt mittels Comptoneffekt. Dieser ist nicht wie der fotoelektrische Effekt von der Ordnungszahl des absorbierenden Gewebes abhängig, sondern nur von dessen (Elektronen-)Dichte. Damit kann eine Überdosierung im Knochengewebe vermieden werden und es ist eine homogene Dosisverteilung in Knochen- und Weichteilgewebe möglich. Hochenergetische Röntgenbestrahlung weist -außerdem eine gute Eindringtiefe auf und erreicht die maximale Dosis erst unterhalb der Hautoberfläche in ca. 1,5 cm Tiefe. Diese Eigenschaft führt bei der Behandlung tiefer liegender Strukturen (z. B. Bestrahlung eines Gehirntumors) zu einer erwünschten Schonung der Haut.
Elektronenstrahlen besitzen im Vergleich zu hochenergetischen Röntgenstrahlen eine geringere Eindringtiefe mit einem wesentlich abrupteren Dosisabfall in der Tiefe. Daher eignen sich Elektronen für die Behandlung oberflächlicher Läsionen (je nach Elektronenenergie bis ca. vier cm Tiefe), insbesondere, wenn diese über kritischen Organen liegen, die geschont werden sollen. Elektronen werden daher z. B gerne bei Läsionen über der Brust- und Bauchwand – insbesondere von Katzen und kleinen Hunden – verwendet (Abb. 1B, C).